Профилактика инсульта
Федин А.И.
Российский государственный медицинский университет, г.Москва
Парадокс болезней заключается в том, что люди, жалуясь на аллергию, боятся рака или СПИДа, а умирают наиболее часто от сердечно-сосудистых заболеваний. По результатам эпидемиологических исследований в России, болезни сердечно-сосудистой системы занимают до 70% всей регистрируемой патологии, причем более 35% в этой группе приходится на цереброваскулярные заболевания. Статистика инсультов весьма удручающая для нашей страны - это касается как распространенности инсульта, так и смертности от него. На рис. 1. представлена смертность от инсульта на 100 тысяч мужчин и женщин в различных странах в 2000г. Анализ смертности от инсульта, проведенный в 40 странах, показал, что Россия имеет самый высокий показатель среди мужчин и женщин после Киргизии. Такая же тенденция характерна для почти всех бывших советских республик.
 |
По данным Е.И.Гусева и соавт., в 2001г. заболеваемость инсультом в России среди лиц старше 25 лет составляла 2,34 на 1000 населения, при этом у мужчин стандартизованный по возрасту показатель равнялся 2,82, у женщин - 2,05.
Общая смертность при инсультах -1,28 на 1000 населения. В старших возрастных группах после 60 лет преобладают заболеваемость и смертность от инсульта у женщин по сравнению с мужчинами. Общая летальность у больных с инсультом в 2001г. составляла 40,3%. Инвалидность с потерей трудоспособности, по разным данным, варьирует от 40 до 80%, но достоверной статистики по этому вопросу в нашей стране нет. Проведенное Е.Б.Белоусовым и соавт. в 2002г. фармакоэкономическое исследование показало, что стоимость стационарного лечения больного с инфарктом мозга составляет 22 тыс. руб., а последующее реабилитационное лечение в течение одного года - 65,4 тыс. руб. Приведенные данные подчеркивают особую актуальность проблемы профилактики инсульта.
В современной эпидемиологии и профилактике неинфекционных заболеваний различают первичную и вторичную профилактику инсульта. Первичная профилактика связана с предупреждением таких основных системных заболеваний, как атеросклероз и гипертоническая болезнь. Для современной медицины - это недостижимая задача вследствие того, что не выявлены непосредственно вызывающие их патогенетические механизмы. Вторичная профилактика предусматривает проведение лечебно-диагностических мероприятий, уменьшающих риск осложнений этих заболеваний, среди которых одно из основных мест занимает инсульт. При вторичной профилактике различают популяционную стратегию и стратегию высокого риска. Популяционная стратегия подразумевает профилактику инсульта в больших популяциях населения вне зависимости от наличия в анамнезе инсульта или других сосудистых заболеваний. Как правило, она направлена на формирование здорового образа жизни, правильного питания, снижение среднего артериального давления в большой популяции организованного населения. Такая стратегия требует разработки и финансирования национальных программ по первичной профилактике инсульта.
Стратегия высокого риска направлена на выявление лиц с высокими факторами риска инсульта и проведение у них соответствующих индивидуальных лечебных мероприятий. Подобная стратегия наиболее распространена, так как требует меньших затрат при хороших результатах. Среди факторов риска выделяют неизменяемые и изменяемые. К первым относят пол, возраст, расовую принадлежность, место проживания и экологические факторы окружающей среды. Имеются определенные взаимоотношения и зависимость заболеваемости инсульта от этих факторов, но повлиять на них нельзя, поэтому они и получили такое название.
Вторые включают артериальную гипертензию (АГ), курение, фибрилляцию предсердий, сахарный диабет, гиперхолестеринемию, снижение физической активности и ожирение, гипергомоцистеинемию, применение оральных контрацептивов, гормонозаместительную терапию в менопаузе и чрезмерное употребление алкоголя. Роль этих факторов неоднозначна, и их изучению посвящены многочисленные корпоративные исследования.
По данным Государственного научного центра профилактической медицины, в 1992-1999гг. распространенность АГ в Российской Федерации в популяции мужчин составляла 39,2%, женщин - 41,1%. О наличии у себя АГ знали 37% мужчин и 60% женщин, из них только 20% мужчин проходили лечение.
При исследовании, проведенном НИИ неврологии РАМН, АГ была обнаружена у 78,2% больных, перенесших острые нарушения мозгового кровообращения. Установлена эпидемиологическая корреляция между заболеваемостью инсультом, повышением систолического (САД) и диастолического (ДАД) давления при всех его типах вне зависимости от возраста и пола. Мета-анализ в 1990г. 9 проспективных исследований, включающих 420 тысяч лиц в течение 10 лет, показал, что риск инсульта увеличивается на 46% при каждом повышении ДАД на 7,5мм рт.ст. В исследовании Multiple Risk Factor Intervention Trial (347 978 мужчин) при максимальных значениях САД (> 151мм рт.ст.) и ДАД (>98мм рт.ст.) риск инсульта, связанный с увеличением САД, в 2 раза превышал риск при росте ДАД. Несмотря на то что частота развития инсульта практически прямо пропорциональна уровню АД, в общей популяции значительно более часто от этого осложнения страдают больные с «мягкой» АГ (при уровне АД от 140/90 до 159/99 мм рт.ст.), которых значительно больше, чем лиц с умеренной и тяжелой АГ. По данным НИИ неврологии, «мягкая» АГ регистрировалась у 56,6% больных, у которых инсульт развился на фоне повышения АД.
В исследовании SHEP, направленном на лечение больных в возрасте старше 60 лет с изолированной САД, выявлено снижение частоты инсульта на 36%, а в исследовании Syst-Eur - на 42%.
Значительное число исследований было посвящено контролю АГ и его влиянию на заболеваемость инсультом в пожилом возрасте. Так, в ходе исследования SHEP проведено лечение в течение 4,5 лет 4736 рандомизированных пациентов старше 60 лет с изолированной САД > 160мм рт.ст. и ДАД < 90мм рт.ст. Выявлено снижение заболеваемости инсультом на 36% при контроле АГ. Все приведенные данные убедительно демонстрируют роль АГ в заболеваемости инсультом и возможность ее эффективного уменьшения при лечении.
Лечение АГ следует начинать с нелекарственной терапии, направленной на снижение избытка массы тела, ограничение потребления насыщенных жиров и поваренной соли, достаточное употребление солей калия, магния, кальция, снижение употребления алкоголя, отказ от курения и использование физические нагрузок динамического типа.
В лечении АГ у практикующих врачей доминирует мнение, что ДАД «легче контролировать». Отношение к САД заключается в том, что его трудно стабилизировать, так как оно подвержено большим колебаниям. В то же время в упомянутых выше исследованиях, направленных на контроль как САД, так и ДАД, выявлено уменьшение частоты инсульта, что свидетельствует о необходимости контроля обоих уровней АД.
Для лечения АГ применяют диуретики, (β-адреноблокаторы, ингибиторы ангиотензин-превращающего фермента, антагонисты кальция, альфа-адреноблокаторы и антагонисты рецепторов ангиотензина. Интересные данные получены в первом Российском фармакоэпидемиологическом исследовании АГ (рис. 2). Как выяснилось, отечественными врачами наиболее часто для контроля АГ применяются ингибиторы АПФ, бета-блокаторы и диуретики, реже - антагонисты кальция и препараты других фармакологических групп.
 |
Согласно данным И.Е.Чазовой, при приеме традиционных гипотензивных средств, риск развития инсульта уменьшается примерно на 38% при этом основные преимущества такой терапии становятся заметными в течение 1-2 лет от ее начала. Исследованиями НОТ установлено, что наименьшей частоте развития инсультов соответствует снижение ДАД до 82,6 и САД до 138,5мм. рт.ст. Однако, по мнению Е.В.Ощепковой, у больных с АГ и цереброваскулярной патологией планирование снижения АД до желаемого уровня должно строиться с учетом компенсаторных возможностей церебральной гемодинамики. В работах З.А.Суслиной показано, что у больных с последствиями инсульта и хронической ишемии мозга ориентиром выраженного нарушения церебральной гемодинамики и гипореактивности сосудов мозга могут служить маркеры в виде экстрапирамидного или псевдобульбарного синдрома, наличие очаговых или диффузных изменений вещества мозга по данным КТ/МРТ головы, стенозы и окклюзии магистральных артерий головы по данным их дуплексного сканирования и ишемическая болезнь сердца. При наличии у больного перечисленных маркеров снижение САД на первоначальном этапе лечения не должно превышать 15%, а ДАД - 10% от стартового уровня. В практике столь незначительное, на первый взгляд, снижение АД составляет ощутимую величину, и в случаях длительного (в течение 3-5 лет) и стабильного снижения АД можно ожидать значительного улучшения отдаленного прогноза. Это еще раз было доказано в ходе международного многоцентрового исследования PROGRESS, результаты которого опубликованы в 2001г. В исследование были включены пациенты, перенесшие инсульт или транзиторную ишемическую атаку (ТИА) на фоне АГ, а также лица с нормальным АД. В течение 4 лет они принимали ингибитор АПФ периндоприл (престариум) в сочетании с диуретиком индапамидом. В целом частота повторного инсульта уменьшилась на 28%, ишемического - на 24%, а геморрагического - на 50% по сравнению с группой плацебо. При этом АД снизилось всего на 9,7/4,0мм рт.ст. от исходного уровня (147/86 мм рт.ст.).
Клиническими критериями эффективности антигипертензивной терапии у больных АГ с сосудистой мозговой патологией являются стабильность АД в течение суток, включая ранние утренние часы, отсутствие гипертонических кризов и достижение устойчивой компенсации имеющихся цереброваскулярных расстройств. Наиболее частыми причинами недостаточно эффективной антигипертензивной терапии являются игнорирование вышеназванных методов нелекарственной терапии, применение неэффективных средств, быстрая смена гипотензивного препарата, использование в начале лечения комбинации препаратов или препаратов центрального действия. Вместе с тем в исследовании PROGRESS было показано, что в 75% случаев инсульт развивается без повышения АД (нормотензивный инсульт). Наиболее частыми причинами нормотензивного инсульта выступают кардиогенная или артерио-артериальная эмболия и атеротромбоз интракраниальных артерий. На их возникновение возможное влияние оказывают другие факторы риска инсульта.
Курение, особенно сигарет, оказывает мультифакторное воздействие на стенки артерий (снижение их эластичности, атероматоз) и показатели крови (увеличение уровня фибриногена, агрегации тромбоцитов и липопротеидов низкой плотности). Подчеркиваются особая высокая взаимосвязь табакокурения и развития атеросклеротического стеноза в сонных артериях. Мета-анализ клинических исследований выявил при курении увеличение риска инсульта в 1,9 раза. У 90% некурящих в сыворотке крови обнаруживается никотин вследствие общения с курящими, что при наличии других факторов риска повышает вероятность развития инсульта почти в 2 раза.
Фибрилляция предсердий служит существенным фактором риска инсульта, что связано с тромбоэмболией мозговых артерий субстратами тромба в полостях левого предсердия или желудочка сердца. Наиболее часто она развивается при ишемической болезни сердца и последствиях инфаркта миокарда, реже - при ревматическом митральном пороке сердца. Более чем в 50% случаев фибрилляция предсердий вызывает тромбоэмболический инсульт. Особое значение имеют «тихие» или бессимптомные эмболические инфаркты мозга (их частота составляет 1-2% среди всех случаев инфаркта мозга), которые в последующем увеличивают риск деменции или других когнитивных расстройств. Риск тромбоэмболического инсульта у больных с фибрилляцией предсердий увеличивается с возрастом при наличии АГ.
Имеются существенные доказательства, что сахарный диабет является важным фактором риска инсульта. Его относительный риск составляет 1,5-3,0 в зависимости от типа и тяжести инсульта. В исследовании Copenhagen City Heart Study сахарный диабет сформулирован как риск инсульта, имеющий самостоятельное значение. В Британском исследовании мужчин показано, что риск инсульта при сахарном диабете увеличивается у пожилых больных с АГ. Лечение сахарного диабета как 1, так и 2-го типа с нормализацией уровня глюкозы в крови уменьшают риск микроваскулярных осложнений - ретинопатии, нефропатии и нейропатии, но не уменьшает риск макроваскулярных осложнений, в том числе инсульта. Однако в ряде исследований отмечено, что интенсивное лечение диабета 2-го типа, сочетающегося с АГ, приводит к уменьшению риска инсульта до 44%.
В многочисленных исследованиях выявлена сильная корреляция риска развития коронарной патологии и дислипидемии (ДЛП), в то время как степень подобной связи с риском инсульта до настоящего времени точно не установлена. К липидам плазмы относят холестерин (ХС), триглицериды (ТГ) и фосфолипиды. Холестерин выполняет важные биохимические функции в человеческом организме. Он необходим для синтеза стероидных и половых гормонов, образования желчи, входит в состав всех клеточных мембран организма. ТГ - это эфиры ЖК и спирта глицерина, которые содержатся в различных липопротеидах (ЛП). Липиды транспортируются в крови в составе сложных надмолекулярных комплексов - ЛП, которые представляют собой водорастворимые липидно-белковые глобулярные структуры, состоящие из молекул белков, свободного ХС, эфиров ХС и фосфолипидов. Белки, входящие в состав ЛП частиц, называют аполипопротеинами, или апобелками, и они выполняют структурную и адресную функции. Благодаря высокоспецифичному взаимодействию между апобелками ЛП и белками-рецепторами на клеточной мембране осуществляется рецепторопосредованное связывание ЛП с клетками. Основными ЛП в зависимости от их плотности, размеров и состава входящих липидов и апобелков являются хиломикроны (ХМ), липопропротеиды очень низкой плотности (ЛПОНП), липопротеиды низкой плотности (ЛПНП), липопротеиды высокой плотности (ЛПВП). ЛПОНП синтезируются в печени, в основном состоят из эндогенных ТГ и в меньшей степени - из эфиров ХС, поэтому их повышенное содержание в плазме крови проявляется гипертриглицеридемией (ГТГ). ГТГ часто диагностируется у больных с инсулиннезависимым сахарным диабетом, гипотиреозом, ожирением. В сочетании с низким уровнем ЛПВП ГТГ служит фактором риска развития атеросклероза.
По данным Н.В.Перовой и других авторов, повышенное содержание в плазме ЛПНП отчетливо связано с развитием коронарного, каротидного и периферического атеросклероза. Однако для того чтобы ЛПНП стали атерогенными, они должны подвергнуться модификации, причиной которой чаще всего служит процесс перекисного окисления ЛПНП. Окисленные ЛПНП изменяют свои свойства в двух направлениях:
сначала нарушается их взаимодействие с рецепторами печени, потом они становятся активными раздражителями для моноцитов. Активированные моноциты крови проникают в субэндотелиальное пространство сосуда, превращаясь в макрофаги, которые фагоцитируют модифицированные ЛПНП и превращаются в пенистые клетки, т.е. клетки, переполненные эфирами ХС. Активированные макрофаги и пенистые клетки высвобождают биологически активные вещества - факторы роста, провоспалительные цитокины, молекулы адгезии. В результате в большей мере усиливаются процессы проницаемости эндотелия и роста атеросклеротической бляшки, что в конечном итоге ведет к сужению просвета сосуда и разрыву покрышки бляшки с образованием внутрисосудистого тромба. Именно ХС ЛПНП с учетом его важной роли в формировании атеросклеротической бляшки является главной мишенью гиполипидемической терапии.
ЛПВП - антиатерогенные ЛП частицы, которые осуществляют обратный транспорт ХС из сосудистой стенки и макрофагов в печень, откуда он выводится из организма в составе желчных кислот. Уровень ХС ЛПВП в плазме имеет обратную зависимость с развитием атеросклероза - чем ниже содержание ХС ЛПВП, тем выше вероятность развития атеросклероза.
В исследовании Multiple Risk Factor Intervention Trial у мужчин выявлена зависимость между летальностью от ишемического инсульта и высоким уровнем ХС. Honolulu Heart Program продемонстрировала прогрессивное одновременное увеличение уровня ХС и частоты тромбоэмболического инсульта. В то же время проведенный в 1995г. мета-анализ, включавший 13 тысяч случаев инсульта среди 450 тысяч наблюдавшихся лиц в 45 проспективных исследованиях, не подтвердил корреляции уровня ХС и частоты инсульта.
Иные данные получены в исследованиях, изучавших связь развития инсульта не только с гиперхолестеринемией, но и с другими показателями липидтранспортной системы. В программе Oxfordshire Community Study продемонстрирована обратная взаимосвязь между значительным снижением уровня ЛПВП и риском транзиторных ишемических атак и «малого» инсульта. В исследовании Northern Manhattan выявлена протективная роль ЛПВП в заболеваемости ишемическим инсультом. В то же время в программе MRFIT показано парадоксальное увеличение заболеваемости инсультом при низком содержании в плазме ХС. Американская образовательная программа холестерина (NCEP) рекомендует при концентрации ЛПВП ниже 40 мг/дл (1,03 ммоль/л) начинать проведение гиполипидемической терапии.
Эффективность гиполипидемической терапии на уменьшение действия факторов риска инсульта была показана в 2000г. при мета-анализе 41 рандомизированного исследования, включавшего 80 тысяч обследованных. В ходе 4-летнего наблюдения при применении гиполипидемической терапии выявлено снижение на 16% заболеваемости как фатальным, так и нефатальным инсультом по сравнению с контрольной группой. В других мета-анализах при назначении статинов отмечено уменьшение риска инсульта от 23 до 30%.
Наиболее значимым было Скандинавское исследование симвастатина по вторичной профилактике инсульта, где в течение 5,4 лет наблюдались 4444 пациента с уровнем холестерина от 5,5 до 8,0 ммоль/л. Симвастатин назначали по 20-40 мг/день. В результате получено снижение риска инсульта по сравнению с группой контроля на 30%.
В соответствии с российскими рекомендациями, разработанными в 2004г. Комитетом экспертов Всероссийского общества кардиологов, терапия ДЛП должна включать немедикаментозные мероприятия по снижению массы тела и назначение гиполипидемических препаратов. Немедикаментозная терапия предусматривает назначение диеты, коррекцию веса, повышение физической активности и прекращение курения.
Основные требования гиполипидемической терапии заключаются в снижении потребления жира до 30% общего количества потребляемых калорий (2000 калорий). Соотношение полиненасыщенных жиров к насыщенным должно составлять 1,5. Рекомендовано включение в диету морской рыбы, содержащей большое количество полезных омега-3-ненасыщенных жирных кислот, овощей и фруктов.
Американский Национальный институт здоровья рекомендует всем лицам, особенно в пожилом возрасте, совершать интенсивные физические упражнения каждый день в течение 30 минут.
К наиболее часто применяемым гиполипидемическим средствам относятся статины (ингибиторы синтеза ХС в печени), фибраты и никотиновая кислота. В настоящее время в России используются следующие препараты из группы статинов: ловастатин (мевакор®), симвастатин (зокор®), правастаин (липостат®), аторвастатин (липримар®) и флувастатин (лескол®). Статины назначают при ДЛП Па, Пb и III типов, они снижают ХС ЛПНП на 20-60%, ТГ - на 10-40% и повышают уровень ХС ЛПВП - на 5-15%. Лечение начинают с небольшой дозы препарата (5-10мг), постепенно повышая ее до оптимальной суточной дозы (20 мг/день). При высоких значениях ХС дозу увеличивают до 40мг, при этом возможны серьезные побочные действия (миопатия, рабдомиолиз).
Безусловными показаниями к применению статинов являются сочетание гипехолестеринемии (общий ХС>5,2 ммоль/л) с гемодинамически значимым стенозом сонной или других артерий, атеросклерозом периферических артерий, аневризмой брюшной аорты, сахарным диабетом или перенесенным атеротромботическим инсультом.
Фибраты и никотиновая кислота показаны при выраженной гипертриглицеридемии с нормальными или незначительно повышенными показателями ХС. Фибраты применяют в следующих дозах: гемфиброзил - 600мг 2-3 раза в день, безафибрат - 200мг 2-3 раза в день, ципрофибрат - 100мг и фенофибрат М - 200мг в день. Фибраты снижают уровень ТГ на 30-50%, ХС ЛПНП - на 10-15% и повышают концентрацию ХС ЛПВП на 10-20%.
Никотиновая кислота в повышенных дозах (3-5г в день) обладает гиполипидемическим действием, уменьшая в равной степени содержание ХС и ТГ. Ее применение часто сопровождается побочными явлениями в виде резкого покраснения лица и верхней половины туловища. При приеме препарата эндурацина (100-200 мг/день) подобные явления наблюдаются редко.
Значимыми для риска инсульта осложнениями атеросклероза являются атеросклеротические бляшки в магистральных мозговых артериях. Впервые в 1905г. Chiari на основании 400 аутопсий показал, что в 4 из 7 случаев атеросклеротических тромбов в бифуркации общей сонной артерии обнаруживаются эмболии в интракраниальных артериях. С этого времени появляются многочисленные публикации о роли эмболии из атеросклеротических бляшек в патогенезе тромбоэмболического инсульта. В отечественной литературе первую фундаментальную работу по проблеме «Стеноз и тромбоз сонных артерий и нарушения мозгового кровообращения» опубликовал в 1963г. Е.В.Шмидт. Наиболее типичны для их локализации участки бифуркации и устья артерий как на экстракраниальном, так и интракраниальном уровнях (рис. 3). Наиболее часто процесс образования атеросклеротических бляшек начинается с бифуркации общей сонной артерии или устья внутренней сонной артерии.
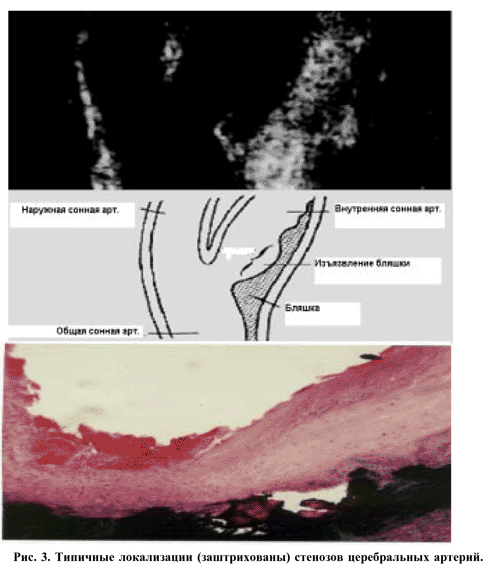 |
По данным А.В. Покровского, частота атеросклероза в развитии стенозов и окклюзии прецеребральных артерий (термин, рекомендованный для применения в МКБ-10, ранее применялся термин «брахиоцефальные артерии») составляет более 80% при среднем возрасте больных от 50 до 60 лет. Частота случаев у мужчин в 4 раза выше, чем у женщин. Более чем у 50% патология ветвей дуги аорты сочетается с артериальной гипертензией. Атеросклероз в прецеребральных артериях чаще всего локализуется в бифуркации общей сонной артерии. Изолированные поражения артерий встречаются гораздо реже, чем множественные. Частота поражения прецебральных артерий примерно такова: бифуркация сонной артерии - 80%, подключичный сегмент - от 10 до 15%, брахиоцефальный ствол и устье левой сонной артерии - от 5 до 10%.
По мнению многих авторов, для уточнения показаний к каротидной эндарэктомии (ЭАЭ) необходимо провести исследования строения и топографии атеросклеротической бляшки в корреляции со степенью стеноза и динамикой церебральной перфузии. Уточнению этого вопроса способствовало внедрение в клиническую практику нового метода ультразвукового исследования сосудов - дуплексного сканирования, которое позволило не только выявлять атеросклеротическую бляшку на раннем этапе ее развития, но и исследовать ее морфологию. Атеросклеротические бляшки по своей морфологии могут быть плоскими и кальцинированными или рыхлыми, с участками изъязвления. Последние бляшки называют гетерогенными. На рис. 4. представлены данные дуплексного сканирования гетерогенной бляшки во внутренней сонной артерии и морфологического исследования после каротидной ЭАЭ.
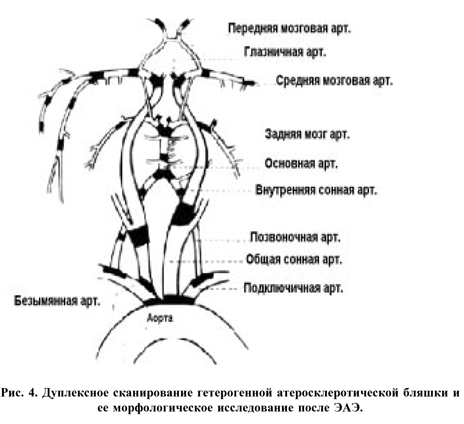 |
Наибольшую опасность для эмболического инсульта представляют гетерогенные бляшки, и поэтому при их выявлении следует обязательно проконсультироваться с ангиохирургом. Помимо этого, данные Роттердамского исследования показали, что при применении дуплексного сканирования увеличение толщины интимы-медии сонных артерий даже в пределах нормальных значений (от 0,75 до 0,91мм) сопровождается увеличением относительного риска первого инсульта в 4,8 раза. Этот фактор риска был самостоятелен и независим от других факторов риска инсульта (мужской пол, возраст, масса тела, курение, сахарный диабет и дислипидемия).
Первая успешная реконструкция общей и внутренней сонной артерии была выполнена в 1951г. в Аргентине. За 50 лет хирургия сонных артерий претерпела бурное развитие. На сонных артериях были выполнены сотни тысяч операций. В США каротидная ЭАЭ - наиболее частый вид всех операций, в том числе сосудистых. Однако почти одновременно с началом внедрения хирургического метода лечения сонных артерий возникла дискуссия между его сторонниками и противниками, которая продолжается до настоящего времени. Ведущие неврологи и ангиохирурги решают два основных вопроса: показания к каротидной ЭАЭ и определение ее эффективности в отношении профилактики инфаркта мозга. При решении вопроса показаний к каротидной ЭАЭ учитываются такие факторы риска, как наличие ИБС, выраженной АГ, риск диагностической ангиографии и, конечно, риск самой операции.
Патология коронарных артерий, по данным некоторых авторов, обнаруживается у больных со стенозом сонных артерий в 25-40% случаев. Это служит обоснованием необходимости тщательного выявления и лечения патологии сердца у лиц, подлежащих каротидной ЭАЭ. Анализ литературных данных, посвященных результатам каротидной ЭАЭ, показал, что в 50-70% случаев смерть больных после операции обусловлена патологией сердца и только в 13-20% - нарушением мозгового кровообращения.
Целесообразность проведения каротидной ЭАЭ определяется степенью стеноза внутренней сонной артерии и клиническими проявлениями заболевания. Большинство клиницистов склоняются в пользу хирургического лечения транзиторных ишемических атак (ТИА). Обращается внимание на тип и локализацию ТИА, исходя из того, что приступы в системе внутренней сонной артерии имеют лучший прогноз, чем другие виды ТИА. По некоторым данным, у больных с ТИА удачная операция снижает риск инсульта до 1-2% в год. Вместе с тем данные анамнеза больных с ТИА свидетельствуют, что без хирургического вмешательства риск инсульта равняется 10% в течение года после возникновения симптоматики и 5-6% через год. Длительные наблюдения показали, что у 85-95% пациентов после каротидной ЭАЭ ТИА прекращаются или наблюдаются значительно реже. Имеются данные о том, что у больных со стенозом внутренней сонной артерии, перенесших инсульт, частота повторного его развития без хирургической коррекции каротидного стеноза достигает 5-20% в год. У больных, которым проводилось хирургическое лечение, этот показатель снижается до 1-2% в год.
В сосудистой хирургии нет проблемы, которая вызывала бы большую дискуссию, чем активная хирургическая тактика при асимптомных поражениях сонных артерий. Безусловно, ни в одном из исследований не отвергается тот очевидный факт, что естественное течение бессимптомных поражений имеет тот или иной риск развития инсульта. Однако ряд авторов полагают, что в большинстве случаев инсульту предшествуют ТИА. На этом основании обосновывается выжидательная тактика - развитие ТИА при исходно бессимптомном течении является показанием к хирургическому лечению. В то же время, по данным НПЦ сердечнососудистой хирургии им. А.Н.Бакулева, в 5,2% случаев эмболический инсульт при бессимптомном стенозирующем поражении внутренней сонной артерии возник без ТИА. Эти факты ставят под сомнение целесообразность выжидательной тактики.
В наиболее полной степени на вопрос о показаниях к каротидной ЭАЭ отвечают международные корпоративные исследования, результаты которых основаны на большом, статистически достоверном и однородном клиническом материале. В двух больших подобных исследованиях - Американском (NASCET) и Европейском (ECST) - при стенозах внутренней сонной артерии (70-99% диаметра артерии) сравнивались результаты каротидной ЭАЭ и медикаментозного лечения. В 70% случаев стенозов с церебральной симптоматикой было показано преимущество хирургического лечения в плане профилактики ТИА и инсультов.
1. Стеноз артерии более 70% (даже при бессимптомном течении или прогрессивно нарастающей неврологической симптоматике).
2. Гетерогенная атеросклеротическая бляшка в бифуркации сонной артерии при любой степени стеноза и выраженности хронической ишемии мозга.
3. Вертебробазилярная недостаточность, обусловленная синдромом «обкрадывания» головного мозга (ретроградный кровоток по позвоночной артерии при окклюзии или резком стенозе устья подключичной артерии).
4. Рестеноз после ЭАЭ или ангиопластики.
В значительном числе работ показана положительная роль антиагрегантной терапии в предотвращении нарушений мозгового кровообращения, профилактике тромбозов и эмболии при стенозах прецеребральных артерий, уменьшении рестенозов после хирургических операций на мозговых артериях. В 1994г. проведен анализ 145 исследований по применению антиагрегантной терапии у 100 тысяч пациентов с риском сердечно-сосудистых заболеваний, из них у 11707 больных в анамнезе был инсульт или ТИА. Мета-анализ в этой подгруппе показал уменьшение заболеваемости нефатальным инсультом на 23% и отсутствие статистически достоверного эффекта на заболеваемость инсультом с летальным исходом.
В современной клинической фармакологии представлены три класса антиагрегантных препаратов. Наиболее широко известна ацетилсалициловая кислота. Основной механизм ее действия связан с необратимой блокадой циклооксигеназы-1. Дипиридамол блокирует обратный захват аденозина (мощного ингибитора агрегации тромбоцитов) и подавляет фосфодиэстеразу, увеличивая локальную концентрацию в клетках циклической АМФ. Тиенопиридины (тиклопидин и клопидогрель) блокируют АДФ-индуцируемую агрегацию тромбоцитов и связывание фибриногена. В рекомендациях Европейского Совета по инсульту, Европейского неврологического общества и Европейской Федерации неврологических обществ (2003г.) содержатся сведения о том, что при вторичной профилактике инсультов применение ацетисалициловой кислоты уменьшает на 13% риск развития повторных инсультов. Дипиридамол в сочетании с ацетисалициловой кислотой снижают риск повторных инсультов на 23% (исследования ESPS и ESPS 2).
Одним из важнейших вопросов применения ацетисалициловой кислоты остается вопрос о величине ее дозировок. В настоящее время доказано, что не существует достоверных различий в эффективности высоких (500-1500мг), средних (160-325мг) и низких (50-75мг) доз ацетилсалициловой кислоты. Эти данные отражаются на различных подходах практикующих неврологов к назначению дозы аспирина. В проведенном в 1998г. анализе (Masuhr et al.) было показано, что в Западной Европе 50,0% неврологов для профилактики повторных инсультов назначают низкие дозы ацетилсалициловой кислоты (от 30 до 175 мг/день), а другая половина - средние (200-400 мг/день). В Северной Америке около 60% врачей предписывают средние дозы и около 40% - высокие (500-1300 мг/день).
Одним из самых тяжелых побочных действиий ацетисалициловой кислоты являются язвы и кровотечения в желудочно-кишечном тракте. В ряде проспективных исследований и их мета-анализе выявлена их частота от 2 до 3%, при этом показано отсутствие дозозависимого действия препарата на частоту геморрагии и осложнений со стороны ЖКТ. Длительное время кардинальным решением этой проблемы считалось использование кишечнорастворимых форм ацетилсалициловой кислоты. Но дальнейшие исследования показали, что применение этих форм не приводило к рубцеванию возникших язв в ЖКТ, в то время как у 90% больных после отмены этих препаратов язвы рубцевались.
В 1989 и 1993гг. было проведено два больших рандомизированных исследования с изучением эффективности тиклопидина по предупреждению повторного ишемического инсульта, в которых выявлены уменьшение риска нефатального инсульта на 23% и отсутствие его статистически значимого влияния на фатальный инсульт. Однако одновременно было показано в 1% случаев развитие тяжелой нейтропении, реже - тромботической тромбоцитопенической пурпуры и других серьезных побочных действий. В связи с этим стал изучаться новый производный тиенопиридина, сходный с тиклопидином, но лишенный его побочных действий - клопидогрель.
В 1996г. были опубликованы результаты большого проспективного исследования CAPRIE, включавшего 19815 пациентов с сердечнососудистыми заболеваниями, их них 6431 перенес ишемический инсульт. Из исследования были исключены больные с кардиэмболическим инфарктом мозга. Сравнивалось действие клопидогреля с аспирином. Исследование показало, что уменьшение повторных случаев инфаркта миокарда и инсульта при применении клопидогреля составляло 5,32%, аспирина - 5,83%. Разница статистически незначима. В подгруппе больных с перенесенным инсультом эти показатели равнялись соответственно 5,2% и 5,7%, разница также была несущественной. Клопидогрель, в отличие от аспирина, не вызывал осложнения со стороны ЖКТ, не было случаев нейропении, в отличие от тиклопидина. Эти данные в дальнейшем были подтверждены в ряде других исследований. Фармакоэкономический анализ, проведенный в 2001г., показал, что стоимость лечения клопидогрелем сопоставима со стоимостью рекомендованного в исследовании ESPS 2 сочетанного лечения аспирином и дипиридамолом. Вместе с тем серьезные побочные действия при лечении клопидогрелем отсутствовали.
В исследовании CURE рекомендовано совместное применение клопидогреля и аспирина у больных нестабильной стенокардией, перенесших инфаркт миокарда или инсульт. Риск повторных инфарктов миокарда и инсульта в этом случае уменьшился на 20%. На основании приведенных данных можно сделать вывод о том, что клопидогрель (препарат плавике рекомендован в однократном приеме разовой дозы 75 мг/день) показан больным, перенесшим инсульт или имеющим ТИА в анамнезе, особенно при признаках нестабильной стенокардии, а также больным, у которых ацетилсалициловая кислота вызывает нежелательные побочные действия.
Уменьшение физической активности является важным, но неоднозначным фактором риска инсульта. Для оценки оптимальной массы тела используется показатель ОМТ = вес в кг/рост в м2. В норме ОМТ находится в пределах 18,5-24,9 кг/ м2. Для оценки избыточной массы тела прибегают также к измерению объема талии (ОТ). В норме у мужчин ОТ не должен превышать 94см, у женщин - 80см. Превышение ОТ у мужчин свыше 102см, а у женщин более 88см служит показателем абдоминального ожирения. В многочисленных исследованиях показано, что постоянная и хорошая физическая активность уменьшает риск ишемической болезни сердца. В ряде программ исследовалось влияние физической активности на риск инсульта. Так, в исследованиях Framiingham Study и Oslo Study у лиц в среднем возрасте выявлено, что постоянная физическая активность приводит к уменьшению риска инсульта у мужчин и в то же время отсутствие статистически значимо не влияет на заболеваемость инсультом женщин в этом возрасте. В большом проспективном исследовании ARIC показано протективное влияние различных видов регулярной физической активности на риск ишемического инсульта.
Активные физические упражнения уменьшают риск инсульта через их влияние на АГ, снижение массы тела и выраженность ишемической болезни сердца. С физической активностью связаны такие биологические факторы, как содержание в крови фибриногена, агрегация тромбоцитов, концентрация ЛПВП и уровень гомоцистеина (ГЦ). В последние годы стала изучаться взаимосвязь между возникновением тромбоза в интрацеребральных артериях и нарушением метаболизма ГЦ. В физиологических условиях происходящие в клетках реакции реметилирования восстанавливают ГЦ до метионина, что обеспечивается ферментом 5-метилтетрагидрофолатом при участии витамина В12. При функциональной недостаточности этого фермента или снижении количества витамина В12 ГЦ элиминируется в межклеточное пространство и кровоток. С учетом его низкой экскреции почками концентрация ГЦ в этих случаях нарастает.
Гипергомоцистеинемия (ГГЦ) может быть самостоятельным началом патологического состояния или следствием развившейся патологии. К первой группе относятся врожденные состояния дефицита ферментной системы клеток, ко второй -заболевания внутренних органов, некоторые общие состояния организма или продолжительное и неблагоприятное воздействие ряда медикаментов, в том числе трициклинических антидепрессантов, дифенина и никотиновой кислоты.
Гипотеза о том, что ГГЦ является фактором риска мозгового инсульта, была сформулирована в 1969г. McCully, который впервые выявил признаки атеросклероза у детей с ГГЦ. В последующие годы интерес к ГГЦ был обусловлен повышенным риском развития у больных мозгового инсульта, кардиоваскулярных заболеваний и венозного тромбоза. В одном ретроспективном исследовании ГГЦ средней степени была выявлена у 42% больных в возрасте до 55 лет с цереброваскулярной болезнью. Увеличение риска инсульта в 4,1 раза при ГГЦ средней степени отмечено в проспективном Британском исследовании мужчин в возрасте 40- 59 лет. Проведенный в научных центрах мета-анализ показал увеличение в 2,5 раза в общей популяции риска развития цереброваскулярных заболеваний. По данным этих исследований, состояние ГГЦ для цереброваскулярных заболеваний оказалось независимым фактором риска их развития. С неменьшей частотой тромботические поражения развивались также в коронарных сосудах, периферических венах и артериях. Особо выделялись в этой возрастной группе риска с умеренной ГГЦ лица, подверженные частым стрессам, курящие и ведущие малоподвижный образ жизни. Статистически значимая связь ГГЦ выявлена с риском развития инсульта и уровнем содержания витаминов. Так, в США в эпидемиологическом исследовании показано, что снижение поступления фолиевой кислоты при ГГЦ увеличивает риск развития инсульта в 1,4 раза.
Взаимосвязь ГГЦ и атеросклероза прослежена при ультразвуковом дуплексном сканировании сонных артерий в случаях повышения ГЦ более 10,5 мкмоль/л. В Фрамингамском проспективном исследовании выявлено статистически значимое увеличение частоты стенозов в сонной артерии более 25% ее диаметра при ГГЦ свыше 14,4 мкмоль/л, при этом одновременно была снижена концентрация фолиевой кислоты и пиридоксина фосфата. Таким образом, ГГЦ лежит в основе развития тромботических цереброваскулярных заболеваний, особенно при высокой концентрации ГЦ.
Для уменьшения действия такого фактора риска, как ГГЦ, умеренное повышение содержания в крови ГЦ (до 25 ммоль/л) следует снизить на 50-60% за счет ежедневного приема 2,5 мг фолиевой кислоты, 25 мг витамина В6 и 40 мкг витамина В12. При тяжелой ГГЦ к этой комбинации рекомендуется добавлять бетаин в дозе 6г в день.
Применение эстрогенсодержащих оральных контрацептивов и терапия эстрогенами женщин в менопаузе приводят к увеличению в плазме крови содержания ЛПВП и уменьшению ЛПНП, что имеет протективное значение для развития атеросклероза, однако при этом одновременно возможны активация гемостаза и гиперкоагуляция крови. Эстрадиол, содержащийся в оральных контрацептивах, увеличивает содержание фибриногена и VII, VIII и X факторов свертывания крови, а также уменьшает уровень физиологических антикоагулянтов (антитромбин III, протеин S). Эти эффекты ухудшают артериальную и венозную гемоциркуляцию. Другой компонент контрацептивов - прогестерон - увеличивает атерогенный потенциал липидов крови. Этим объясняется увеличение риска инсульта у женщин детородного возраста при применении оральных контрацептивов и в менопаузе - при терапии эстрогенами.
По данным ряда исследований, риск инсульта при использовании оральных контрацептивов увеличивается у женщин в возрасте старше 35 лет при курении, артериальной гипертонии и сахарном диабете, при этом наиболее неблагоприятно сказывается содержание дозы эстрогенов в контрацептиве в 50мг (Nurses Health Study). В исследовании RCGP показано отсутствие увеличения риска инсульта при назначении оральных контрацептивов в дозе эстрогенов менее 50мг, у некурящих женщин без АГ.
За последние 20 лет проведено 18 многоцентровых исследований по изучению роли гормонзаместительной терапии у женщин в менопаузе. Показано уменьшение степени гиперхолестеринемии, но без влияния на риск инсульта (Nurses Health Study). Риск ишемического инсульта у женщин в менопаузе увеличивается в 2,6 раза, при этом эффект гормонзаместительной терапии статистически незначим (Framingham Heart Study). По данным некоторых проспективных исследований, возможно увеличение тромбообразования при длительных курсах этой терапии.
В ряде исследований выявлен нейропротективный эффект малых доз алкоголя (80мл в день крепких напитков), связанный с увеличением в крови уровня ХС ЛПВП и эндогенного активатора тканевого плазминогена. На рис. 5. приведена диаграмма влияния различных доз алкоголя на относительный риск инсульта и количество алкоголя (граммы) в различных напитках. Незначительные дозы алкоголя в день (до 12г) незначительно снижают относительный риск инсульта, в то время как в дозе 24г и выше резко его увеличивают. Одновременно обнаружен дозозависимый эффект алкоголя на риск развития геморрагического инсульта (Honolulu Heart Program), при этом дозы крепких напитков более 200мл в день повышают риск инсульта. Причинами этого являются гиперкоагуляция, аритмии, АГ, вызываемые частым употреблением больших доз алкоголя.
 |
Таким образом, при внедрении национальных программ, направленных прежде всего на лечение АГ, формирование здорового образа жизни и медицинской культуры населения, правильном методическом подходе врача к оценке и воздействию на индивидуальные факторы риска профилактика инсульта становится во многих случаях вполне реальной.
Федин А.И. Профилактика инсульта // Неврологический вестник. - 2005. - Т. XXXVII, вып. 1-2. - С.93-104.





