Клинико-нейропсихологические характеристики миофасциального болевого синдрома у больных паркинсонизмом
Байрамова Л.Н., Иваничев Г.А., Гайнутдинов А.Р.
Казанская государственная медицинская академия
Реферат. С целью сравнения клинико-нейропсихологических особенностей миофасциального болевого синдрома больных с разными формами паркинсонизма проведено клиническое обследование 68 пациентов с акинетико-ригидной и преимущественно дрожательной формой с миофасциальным болевым синдромом. Нейропсихологическое тестирование выполнено 22 больным. Выявлены совпадение стороны дебюта паркинсонизма и преимущественной мышечной болезненности примерно у 2/3 больных обеих групп, высокая частота миофасциальных триггерных пунктов в большой грудной (46,5%), ромбовидной (53,8%) мышцах в группе с акинетико-ригидной формой и в горизонтальной порции трапециевидных мышц (82%), мышцах верхнешейного отдела (50%) в группе с дрожательной формой. Первая группа больных характеризовалась достоверно более высокими показателями: индекса мышечного синдрома и активности, толерантности к боли, тенденцией к более высокому мышечному тонусу, увеличению частоты депрессивных нарушений. Выявлен ряд клинических особенностей миофасциальных гипертонусов.
Паркинсонизм - наследственно-дегенеративное заболевание центральной нервной системы, возникающее при поражении базальных ганглиев. Проведенное комплексное клинико-электрофизиологическое исследование головного мозга у 80 больных паркинсонизмом выявило качественную неоднородность при преимущественно дрожательной (ДФ) и акинетико-ригидной формах (АРФ) паркинсонизма, что подтверждалось данными компьютерной томографии головного мозга [9]. В структуре паркинсонизма большинство авторов выделяют АРФ и преимущественно ДФ формы паркинсонизма [3, 7, 11].
Считается, что болевой синдром является частой характеристикой паркинсонизма [4,3,7,11, 13] и может наблюдаться у 10-29% больных паркинсонизмом [16, 17]. Некоторые авторы предлагают разделить все алгические феномены, существующие при паркинсонизме, на миофасциальные, сенсорные, дистонические, связанные с осложнениями лечения леводопосодержащими препаратами (боль on-off периода), смешанные [15, 18]. Важное место в структуре болевого синдрома при паркинсонизме занимает миофасциальный болевой синдром (МФБС), клинико-нейропсихологические особенности которого на сегодняшний день остаются практически неизученными. Вместе с тем болезнь Паркинсона часто манифестирует депрессией, которая может возникать даже раньше явлений паркинсонизма [8]. Депрессия также является важнейшим предрасполагающим фактором и для развития хронической боли, и для трансформации эпизодических болей в хронические [15].
Целью нашего исследования являлась сравнительная характеристика клинико-нейропсихологических особенностей больных АРФ и преимущественно ДФ формами паркинсонизма с сопряженным МФБС.
Был обследован 91 больной паркинсонизмом в возрасте от 23 до 98 лет. У 68 (75%) больных обнаружен МФБС: группа АРФ (женщин - 9, мужчин - 16) и группа ДФ (женщин - 21, мужчин - 22).
В группе АРФ распределение по стадиям паркинсонизма по Хен-Яру выглядело следующим образом: стадия 1.0. была выявлена у 9 (36%) больных, 1.5. - у 1 (4%), 2.0. - у 5 (20%), 2.5 - у 1 (4%), 3.0. - у 6 (24%), 4.0. - у 3 (12%), в группе ДФ: стадия 1.0. - у 11 (25,6%), 1.5. - у 8 (18,6%), 2.0. - у 11 (25,6%), 2.5 - у 5 (11,6%), 3.0. - у 7 (16,3%), 5.0. - у 1 (2,3%).
Нейропсихологическое исследование (тестирование по шкале Бека) было проведено у 22 больных паркинсонизмом с наличием сопряженного МФБС (10 - с АРФ, 12 - с ДФ).
Наряду с общеневрологическим обследованием, базисной оценкой тяжести заболевания, выявления характера и выраженности паркинсонических симптомов [3], нами осуществлялось мануальное тестирование мышц шеи, плечевого пояса и туловища. Для количественной характеристики мышечного синдрома был использован индекс мышечного синдрома (ИМС). Различали три степени тяжести ИМС: I (легкая) - до 5 баллов, II (средняя) - от 5 до 12, III (тяжелая) - более 12. Степень активности миофасциальных триггерных пунктов (МФТП) определяли с помощью феномена вибрационной отдачи (ФВО) [1, 12], уровень болезненности мышц - с помощью тензоальгезиметра Фишера. Для количественного исследования тонуса трапециевидных мышц применялся миотонометр-эластомер в модификации Г.А. Иваничева [5, 6].
Результаты обрабатывали на персональном компьютере с использованием программы «Microsoft Exel-2000» и прикладной программы «Biostat». При анализе распределений количественных признаков использовали критерий Стьюдента. Распределения качественных признаков сравнивали на основе анализа таблиц сопряженности с помощью критерия χ2, точного критерия Фишера [2].
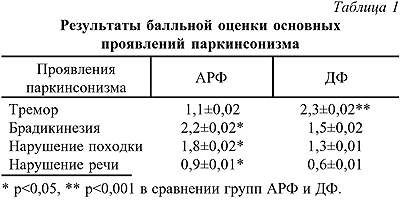
Тремор, ригидность и гипо(а)кинезия являлись ведущими жалобами всех больных с паркинсонизмом: достоверное превышение показателей брадикинезии (р<0,05), нарушений походки (р<0,05) и речи (р<0,05) было выявлено для группы АРФ, показатель тремора был выше в группе ДФ (р<0,001) (табл.1).
 |
Боли в грудной клетке были обусловлены преимущественно МФТП в больших грудных мышцах, которые были обнаружены у 46,5% больных паркинсонизмом в группе АРФ и у 32,5% - в группе ДФ (р<0,05). Боли по задней поверхности шеи были вызваны МФТП в мышцах верхнешейного отдела (ременной мышце головы и шеи, большой и малой прямых, верхней и нижней косых мышцах головы) в группе АРФ - у 33,3%, ДФ - у 50% (р<0,05). В мышце, поднимающей лопатку, МФТП имели место у 29,5% больных паркинсонизмом в группе АРФ и у 19% с ДФ (р>0,05). В надплечьях боли в значительной степени были обусловлены МФТП в горизонтальной порции трапециевидных мышц: в группе АРФ - 61%, в ДФ - 82% (р<0,01). Паравертебральные боли вызывались МФТП, локализованными на грудном уровне в ромбовидных мышцах: у 53,8% с АРФ и 34% с ДФ (Р<0,05). На поясничном уровне МФТП были локализованы в ротаторах позвоночника и квадратной мышце поясницы: при АРФ - у 11% больных, при ДФ - у 10% (р>0,05).
Проведенные исследования выявили также ряд клинических особенностей миофасциальных гипертонусов:
1. При АРФ путем кинестезической пальпации сложнее идентифицировать центральную и периферическую часть МФТП вследствие ригидности мышцы. При ДФ пальпируется только центр МФТП, периферическая часть маскируется гиперкинезом мышцы.
2. При АРФ слабо выражен локальный судорожный ответ, при ДФ же локальный ответ визуально фиксируется плохо, пальпаторно - лучше.
3. Отраженная боль резко определяется при АРФ, в меньшей степени - при ДФ.
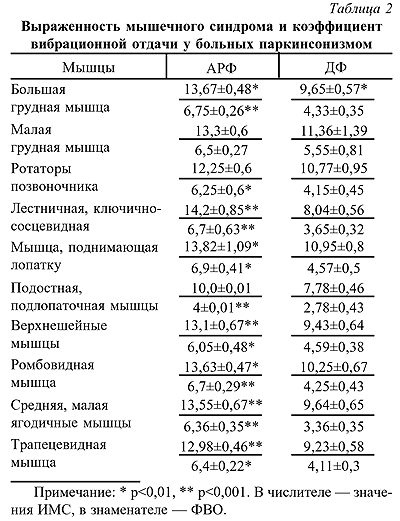
С целью более детального изучения МФБС, были рассчитаны ИМС и степень активности МФТП, которая оценивалась при помощи ФВО. Во всех обследованных мышцах ИМС и ФВО были достоверно выше в группе АРФ, чем в группе с ДФ. В группе АРФ тяжелая степень мышечного синдрома была выявлена практически во всех обследованных мышцах, особенно в мышце, поднимающей лопатку, лестничных и грудино-ключично-сосцевидных. Активность МФТП была наиболее высокой в мышце, поднимающей лопатку, большой грудной, ромбовидной мышцах. Результаты оценки ИМС и коэффициента ФВО у больных паркинсонизмом с сопряженным МФБС представлены в табл. 2.
 |
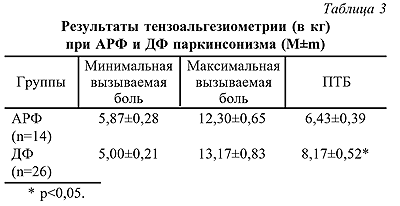
Для объективизации болевых ощущений у больных паркинсонизмом была применена тензоальгезиометрия. Вызываемую болезненность измеряли тензоальгиметром Фишера в горизонтальной порции трапециевидной мышцы. Для выявления переносимости боли был использован показатель толерантности к боли (ПТБ), который вычисляется как разница между максимальными и минимальными значениями. Анализ представленных в таблице 3 данных показал достоверное превышение показателей ПТБ в группе АРФ (р<0,05). Результаты тензоальгезиометрии выявили тенденцию к лучшей переносимости боли в группе ДФ.
С целью объективизации изменений тонуса поперечно-полосатых мышц была проведена миотонометрия. Усредненный показатель тонуса (УПТ) вычислялся на основании полученных значений по формуле: УПТ = (тонус справа + тонус слева)/2, при давлении в 2, 3, 4 кг.
Чем ниже УПТ, тем выше тонус обследуемой мышцы. Анализ результатов исследования показал тенденцию к более высокому тонусу в группе АРФ при сравнении с ДФ. Однако достоверных межгрупповых различий в значениях УПТ выявить не удалось (табл. 4).
При сравнительном анализе АРФ и ДФ было обнаружено, что частота депрессивных нарушений при исследовании по шкале Бека была выше в группе АРФ (соответственно 70% и 33,4%; р<0,05). Достоверные различия в уровне депрессивных нарушений (соответственно 18,8±2,7 и 16,7±1,9 балла) отсутствовали. Обнаружена корреляция между порогом боли и выраженностью депрессии (соответственно г= -0,58 и г= -0,61) для АРФ и ДФ.
Считается, что болевой синдром является частой характеристикой паркинсонизма, при этом имеются единичные сообщения, свидетельствующие о миофасциальном характере болевого синдрома. При клиническом обследовании нами было выявлено, что важная роль в патогенезе и оформлении клинической картины болевого синдрома у больных паркинсонизмом принадлежит МФТП. Совпадение стороны дебюта паркинсонизма и преимущественной мышечной болезненности обнаружено примерно у 2/3 больных обеих групп (АРФ - 67,4%, ДРФ - 68%).
Обращают на себя внимание различия в клинико-нейропсихологических характеристиках МФБС у больных с АРФ и преимущественно ДФ паркинсонизма:
1. Для АРФ выявлена высокая частота МФТП в большой грудной (р<0,05), ромбовидной мышцах (р<0,05). Для ДФ характерна высокая частота МФТП в горизонтальной порции трапециевидной мышцы (р<0,01) и мышцах верхнешейного отдела (р<0,05).
2. ИМС и активность МФТП во всех мышцах были достоверно выше в группе АРФ.
3. Показатель толерантности к боли был выше в группе АРФ (р<0,05).
4. Тенденция к более высокому тонусу обнаружена в группе АРФ.
5. Частота депрессивных нарушений при исследовании по шкале Бека была выше в группе АРФ.
6. Выявлен ряд клинических особенностей миофасциальных гипертонусов, принимающих участие в оформлении клинической картины болевого синдрома у больных АРФ и ДФ паркинсонизма.
Таким образом, результаты исследования позволяют заключить, что МФТП участвуют в оформлении алгического синдрома при паркинсонизме. При изучении МФБС у больных паркинсонизмом необходимо учитывать форму заболевания и оценивать не только клинические, но и нейропсихологические характеристики, которые показывают переносимость пациентом боли и его способность справляться с нею. Это, в свою очередь, требует учета данного фактора при формировании комплекса лечебных мероприятий больных паркинсонизмом с сопряженным МФБС.
Литература
1. Веселовский В.П. Практическая вертеброневрология и мануальная терапия - Рига, 1991.
2. Гланц С. Медико-биологическая статистика - М.: Практика, -1998.
3. Голубев В.Л., Левин Я.И.. Вейн А.М. Болезнь Паркинсона и синдром паркинсонизма - М.: Медпресс, 1999.
4. Дехтерев В.В. Дрожательный паралич - М., 1927.
5. Иваничев Г. А. Миофасциальный генерализованный болевой (фибромиальгический) синдром - М., 2002.
6. Иваничев Г.А., Иваничева Н.А., Есин Р.Г., Инеева Т.И. Переменно-дискретная тонометрия в оценке эффективности постизометрической релаксации локальных мышечных гипертонусов // Журн. неврол. и психиатр. им. СС. Корсакова - 1985 - №1. - С.519-523.
7. Каменецкий В.К. Паркинсонизм. СПб.: Питер, 2001.
8. Крыжановский Г.Н., Карабань И.Н., Магаева С.В. и др. Болезнь Паркинсона (патогенез, диагностика, лечение, профилактика) - М.: Медицина, 2002..
9. Поверетова И.Е. Клинико-электрофизиологические корреляции различных форм паркинсонизма. /И.Е. Повереннова, P.M. Балаклеец, А.С. Балаклеец /Тезисы VIII Всероссийского съезда неврологов, Казань, 21-24 мая 2001. - С.363-364.
10. Роменская Л.Х. Вопросы эпидемиологии, клиники и фармакотерапии паркинсонизма. / Л.Х. Роменская: Автореф. дисс. ... канд. мед. наук. - М., 1976.
11. Столярова Л.Г. и др. Реабилитация больных паркинсонизмом. - М.: Медицина, 1979.
12. Хабиров Ф.А., Хабиров Р. А. Мышечная боль - Казань, 1995.
13. Chudler Е.Н. The role of the basal ganglia in nociception and pain. / E.H. Chudler, W.K. Dong // Pain. - 1995. Jan. - 60(1). - P.3-38.
14. Fields H. Depression and pain: a neurobiological model. / H. Fields //Neuropsechol. Behav. Ther. - 1991. - Vol. 4. - P.83-92.
15. Quinn, N.P., Koller, W.S., Lang, A.E. et al. Painful Parkinson's disease. //Lancet. - I (1986). - P.1366-1369.
16. Rajput A.H. Frequency and cause of Parkinson's Disease.// Can. J. Neurol. Sci. - 19 (1992). - P.571-595.
17. Snider, S.R., Sandyk, R. Sensory Dysfunction. /In W.S. Koller (Ed.), Handbook of Parkinson's Disease. - Markel Dekker. - N.-Y. - 1987. - P.171-180.
18. Tisson F. Wenning G.K., Volonte M.A. et al. Pain in multiple system atrophy // J. Neurol. - 1996. - Feb. - 243(2). - P.153-156.
Байрамова Л.Н., Иваничев Г.А., Гайнутдинов А.Р. Клинико-нейропсихологические характеристики миофасциального болевого синдрома у больных паркинсонизмом // Неврологический вестник. - 2005. - Т. XXXVII, вып. 1-2. - С.18-21.