Роль однофотонной эмиссионной компьютерной томографии с 99mТс-ГМАПО в нозологической диагностике паркинсонизма
Левин О.С., Амосова И.А., Поцыбина В.В., Смоленцева И.Г., Олюнин Д.Ю.
Центр экстрапирамидных заболеваний МЗ СР РФ, Российская академия последипломного образования, г.Москва
Реферат. С помощью однофотонной эмиссионной компьютерной томографии с 99mТс-ГМАПО были обследованы 44 пациента с паркинсонизмом. Клинико-неврологическое исследование проводилось согласно общепринятой методике, включая также количественную оценку выявленных нарушений с помощью шкалы Хен и Яра и унифицированной шкалы болезни Паркинсона (3 версия). Для оценки когнитивных функций применялась шкала деменции Маттиса. Поведенческие нарушения оценивали с помощью специально разработанной шкалы, предусматривавшей рейтинговую оценку 10 наиболее часто встречающихся вариантов поведенческих расстройств. Проведенное нами исследование показало, что данные однофотонной эмиссионной компьютерной томографии в комплексе с клиническими и нейропсихологическими данными могут иметь важное дифференциально-диагностическое значение при нозологической диагностике паркинсонизма, особенно на ранней стадии его развития.
Паркинсонизм относится к числу наиболее частых неврологических синдромов и является одной из основных причин инвалидизации пожилых лиц [1, 7, 8, 16]. Его распространенность, по данным разных исследований, варьирует от 84 до 775 случаев на 100 тысяч населения и быстро нарастает с увеличением возраста. Паркинсонизмом страдают 1-3% лиц старше 65 лет, а риск заболеть им в течение жизни составляет около 4% [21, 26]. Он может быть проявлением нескольких десятков заболеваний головного мозга. В последние десятилетия представления о нозологической структуре паркинсонизма существенно изменились [6, 9, 12, 30]. Эпидемиологические и клинико-патоморфологические исследования доказали, что самой частой причиной паркинсонизма является болезнь Паркинсона (БП), на долю которой приходится 70-80% случаев этого синдрома [1,7, 29]. Около 10-20% случаев паркинсонизма вызваны мультисистемными дегенерациями ЦНС - гетерогенной группой наследственных и спорадических заболеваний, клинически характеризующихся сочетанием паркинсонизма с деменцией (БПД) с вегетативной недостаточностью, мозжечковой атаксией, пирамидным синдромом, глазодвигательными нарушениями или расстройством высших мозговых функций («паркинсонизм-плюс») [4, 35, 48]. Представителями этой группы являются прогрессирующий надъядерный паралич (ПНП), мультисистемная атрофия (MCA), болезнь диффузных телец Леви, или деменция с тельцами Леви (ДГЛ), кортикобазальная дегенерация [6,34,48,52].
В последние годы благодаря клинико-патоморфологическим исследованиям удалось разработать клинические критерии, делающие возможным прижизненную диагностику многих заболеваний из этой группы [35]. Однако отсутствие надежных объективных маркеров БП и мультисистемных дегенерации вызывает трудности при их дифференциальной диагностике, особенно на ранней стадии заболеваний, когда их клинические проявления бывают похожими [16].
По данным Quinn (1994), в 25% случаев прижизненный диагноз БП оказывается ошибочным [44]. В последние годы точность диагностики БП повысилась, однако даже в специализированных центрах, занимающихся проблемой паркинсонизма, ошибочным оказывается каждый десятый диагноз БП. Еще чаще ошибки допускаются при диагностике мультисистемных дегенерации. Проведенные в последние годы исследования показали, что даже в специализированных центрах, занимающихся проблемой паркинсонизма, прижизненный диагноз этих заболеваний оказывается точным только примерно в 70% случаев [35].
Клинические данные в комбинации с результатами структурной нейровизуализации не всегда позволяют правильно поставить этиологический диагноз у больного паркинсонизмом, особенно на ранней стадии заболевания [2, 16, 17, 49]. В связи с этим важное диагностическое значение приобретают методы функциональной нейровизуализации [15, 18, 19, 22, 36, 46, 51].
Сложные дорогостоящие методы функциональной нейровизуализации с введением радиофармпрепаратов, являющихся маркерами пресинаптических или постсинаптических структур дофаминергических стриарных синапсов, нередко позволяют поставить диагноз на ранней стадии заболевания, однако их способность дифференцировать различные заболевания, вызывающие синдром паркинсонизма, остается ограниченной [16, 32, 40].
Однофотонная эмиссионная компьютерная томография (ОФЭКТ) с 99mТс-гексаметил-пропиленеамин-оксимом (ГМАПО) дает возможность исследовать перфузию и тем самым косвенно оценить функциональное состояние различных отделов головного мозга, и прежде всего коры [20]. Это может иметь важное значение для дифференциальной диагностики нейродегенеративных заболеваний со сходной клинической картиной, но различающихся паттерном функционального вовлечения различных мозговых структур [41].
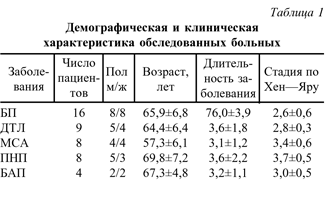
С помощью ОФЭКТ с 99mТс-ГМАПО мы обследовали 44 пациента с паркинсонизмом, в том числе 16 больных БП, диагностированной в соответствии с критериями Банка мозга общества БП Великобритании [24], 9 больных ДТЛ, выявленной по критериям McKeith et al. (1998) [38], 8 больных MCA по критериям Oilman et al., (1998) [25], 8 больных с ПНП по критериям NINDS-SPSP [33], 4 пациентов с болезнью Альцгеймера (БАП) по критериям NINCDS-ADRDA [39] и паркинсонизмом нелекарственной природы. Демографическая и клиническая характеристика обследованных пациентов представлена в табл. 1.
Контрольную группу составили 18 лиц (средний возраст - 55,7±4,8 года), не имевших неврологических или нейропсихологических симптомов, указывающих на заболевание головного мозга.
Клинико-неврологическое исследование проводилось согласно общепринятой методике, но включала также количественную оценку выявленных нарушений с помощью шкалы Хен и Яра [28] и унифицированной шкалы БП (Unified Parkinson's Disease Rating Scale - UPDRS), 3 версия [23]. Для оценки когнитивных функций применялась шкала деменции Маттиса (ШДМ) [37]. ШДМ представляет собой набор когнитивных тестов, оценивающих различные когнитивные сферы, в частности внимание (тест на повторение цифр), инициацию и персеверацию (выполнение альтернирующих движений), конструктивный праксис (копирование рисунков), концептуализация (нахождение обобщающих слов), вербальную и невербальную кратковременную память (например, воспроизведение предложений, узнавание рисунков). Суммарная оценка колеблется от 0 до 152 баллов.
В соответствие с ШДМ у 7 пациентов с БП (средний возраст - 68,2± 6,9 года, длительность заболевания - 6,2±4,4 года, средняя оценка по шкале Хен-Яра - 2,9±0,4) диагностирована деменция (оценка по шкале - ниже 115 баллов). У остальных 9 пациентов с БП (средний возраст - 63,6±5,7 года, длительность заболевания - 5,8±3,4 года, средняя оценка по шкале Хен-Яра-2,5±0,4) когнитивные нарушения не достигали степени деменции (оценка по шкале колебалась от 115 до 129 баллов).
Поведенческие нарушения оценивали с помощью специально разработанной шкалы, предусматривавшей рейтинговую оценку 10 наиболее часто встречающихся вариантов поведенческих расстройств (агрессивность, апатия, аспонтанность, истощаемость, навязчивость, «полевое» поведение, раздражительность, расторможенность, тревожность, эйфория). По 5-балльной шкале (от 0 до 4 баллов) отдельно судили о выраженности и частоте каждого вида поведенческих расстройств [2].
ОФЭКТ проводилась на эмиссионном компьютерном томографе GCA-8500A «Тошиба» спустя 12-15 минут после в/в введения 555 мБк с 99mТс-ГМАПО (церетек) с использованием среднеэнергетического параллельного
коллиматора и получением аксиальных, сагиттальных и коронарных срезов. Перфузию оценивали в лобной, теменной, затылочной, височной долях, стриатуме, таламусе и мозжечке. Данные ОФЭКТ изучали с помощью визуальной 4-балльной рейтинговой шкалы: 0 баллов - перфузия соответствует норме, 1 - снижение перфузии минимальное (сомнительное), 2 - выраженное (явное), 3 - резко выраженное [2].
Статистическую обработку проводили с помощью программного пакета Statistica 6.0 с использованием критерия Стъюдента, критерия согласия χ2, критерия U, непараметрического критерия знаков, рангового корреляционного анализа (по Спирмену).
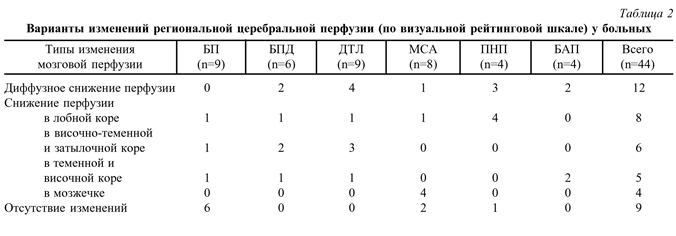
Изменения перфузии тех или иных отделов мозга выявлены у 35 (79,5%) из 44 больных с паркинсонизмом. На основе анализа полученных данных выделено 5 типов изменений церебральной перфузии (табл. 2): 1) диффузное снижение церебральной перфузии; 2) снижение церебральной перфузии преимущественно в лобных отделах при относительной сохранности перфузии в задних отделах больших полушарий; 3) снижение перфузии преимущественно в задних отделах больших полушарий (височной, теменной, затылочной коре) при ее относительной сохранности в лобной коре; 4) снижение перфузии в основном в теменных и височных отделах при относительной сохранности перфузии в лобной и затылочной коре; 5) избирательное снижение перфузии в мозжечке при относительной ее сохранности в полушарных структурах.
Во всех случаях изменения носили двусторонний характер, причем резко выраженной асимметрии церебральной перфузии не отмечено ни у одного из обследованных.
Изменений церебральной перфузии не выявлено у 9 больных с паркинсонизмом, в том числе у 6 с БП без деменции (67%), у 2 с МСА (25%) и только у одного с ПНП (12,5%). В то же время ни в одном случае БПД, ДТЛ и БА с паркинсонизмом не выявлено нормальной картины. Чаще всего - у 12 (27%) - отмечалось диффузное снижение перфузии: оно было выявлено в трети случаев БПД, у 44% с ДТЛ и 50,0% БА с паркинсонизмом. Реже диффузное снижение перфузии отмечалось при ПНП (33%) и МСА (12,5%). В то же время оно не отмечено ни в одном случае БП без деменции (рис. 1.А).
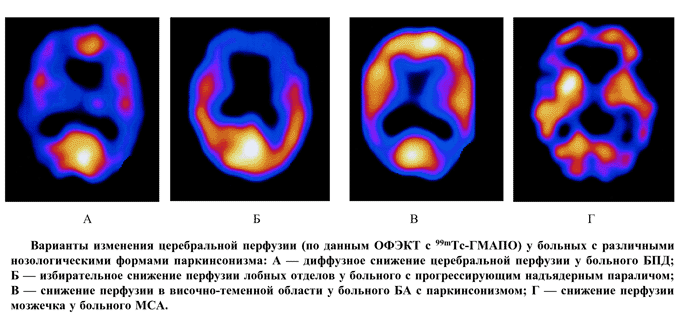 |
В 3 случаях БП без деменции, когда ОФЭКТ выявляло снижение перфузии (преимущественно в лобных, височно-теменных или височно-теменно-затылочных отделах) у больных были обнаружены умеренные нейродинамические и регуляторные когнитивные изменения. Преимущественно двустороннее снижение церебральной перфузии в лобной коре имело место у 8 (18%) больных с паркинсонизмом (рис. 1.Б). Оно было наиболее характерно для ПНП (50%), однако встречалось также при БП без деменции (11%), БПД (17%), МСА (12,5%) и ДТЛ (11%). Ни в одном случае БА с паркинсонизмом избирательное снижение перфузии в лобной коре не отмечалось.
Снижение перфузии преимущественно в задних отделах коры больших полушарий (височной, теменной, затылочной коре) было выявлено у 7 (16%) больных с паркинсонизмом: наиболее выражение при БПД (33%) и ДТЛ (33%), но также у одного больного с БП без деменции (11%). Подобный тип изменений не наблюдался ни в одном случае МСА и БА с паркинсонизмом.
В височно-теменных отделах перфузия была снижена в 5 (11%) случаях, особенно при БА с паркинсонизмом (50%), но имело место также в одном случае БПД (17%), ДТЛ (11%) и одном случае (11%) БП без деменции (рис. 1 В). В то же время данный тип изменений не отмечен ни в одном случае МСА и ПНП.
Наиболее редкий тип изменений - снижение перфузии преимущественно в мозжечке при отсутствии существенных ее изменений в коре больших полушарий - было характерно для МСА (50%) и не встречалось ни при одном другом заболевании (рис. 1 Г). При этом в 2 случаях преобладало снижение перфузии в срединных структурах мозжечка и в 2 - диффузное снижение перфузии мозжечка.
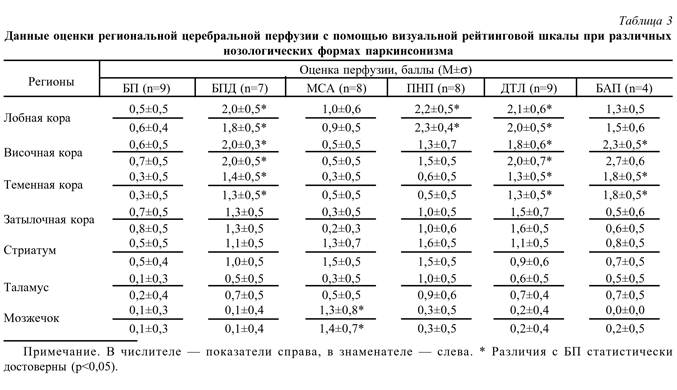
Данные оценки церебральной перфузии с помощью визуальной рейтинговой шкалы в основном соответствовали вышеуказанным результатам (табл. 3). В сравнении с БП более низкая перфузия в лобных долях отмечена при ПНП, БПД и ДТЛ, однако достоверных различий между ними выявить не удалось.
Достоверное снижение перфузии височной коры по сравнению с БП без деменции отмечено при БА с паркинсонизмом, БПД и ДТЛ. Хотя степень снижения перфузии при БА была выше, чем при БПД и ДТЛ, это различие не достигало статистически достоверного уровня. Аналогичные результаты получены и в отношении перфузии теменной коры.
Перфузия в затылочной коре при ДТЛ, БПД и БП без деменции была ниже, чем при МСА, ПНП и БА, а при ДТЛ и БПД - ниже, чем при БП без деменции, однако ни одно из этих различий не было статистически значимым. Между всеми обследованными группами не выявлено также существенных различий в перфузии стриатума и таламуса. В то же время у больных с МСА перфузия мозжечка была достоверно ниже, чем при всех других заболеваниях.
У больных БП без деменции отсутствовали статистически значимые корреляции межу показателями региональной церебральной перфузии, с одной стороны, и возрастом, длительностью заболевания, выраженностью двигательного и нейропсихологического дефекта - с другой.
Характерным для МСА типом нейровизуализационных изменений явилось снижение перфузии мозжечка, которое коррелировало с наличием мозжечковых знаков (r=0,3; р<0,05) и показателем субшкалы ШДМ, оценивавшей внимание (r=0,4; р<0,05). Уровень перфузии в стриатуме при МСА был ниже, чем при БП, но это различие не достигало порога статистической значимости (р=0,1). Показатели церебральной перфузии при МСА не коррелировали с выраженностью поведенческих нарушений.
Основным изменением при ПНП, выявленным у 7 из 8 больных, было двустороннее снижение перфузии лобной коры, причем в 4 случаях оно было относительно избирательным, а в 3 других сочеталось с гипоперфузией височно-теменных и затылочных отделов больших полушарий. Снижение перфузии височной коры отмечалось у 4 больных, а снижение перфузии теменной и затылочной коры - у 2.
Уровень перфузии лобной коры при ПНП оказался достоверно ниже, чем при БП без деменции (р<0,01) и МСА (р<0,05), но не отличался от этого показателя при БПД и других
исследуемых заболеваниях. Кроме того, по сравнению с БП при ПНП оказался ниже захват ГМАПО в стриатуме (р=0,1) и таламусе (р=0,08), тем не менее эти различия не достигали порога статистической достоверности.
У больных ПНП прослеживалась корреляция между региональной перфузией в лобной коре и показателями субшкал ШДМ, оценивавших инициацию, персеверацию (r=0,4; р<0,05) и концептуализацию (r=0,3; р<0,05), а также между показателями по шкале поведенческих нарушений (r=0,4; р<0,01). Снижение перфузии в подкорковых структурах и таламусе при ПНП не коррелировало с выраженностью двигательных или нейропсихологических нарушений. Вместе с тем выявлена тенденция к корреляции между выраженностью поведенческих изменений и состоянием региональной перфузии теменной коры (r=0,4; р=0,1). Таким образом, более тяжелые поведенческие нарушения (в частности «полевое поведение» и расторможенность) чаще наблюдались у пациентов с относительно сохранной перфузией теменной коры.
У больных БПД выявлено 4 типа изменений: 1) диффузная гипоперфузия (33%); 2) гипоперфузия в височно-теменной и затылочной коре (33%); 3) гипоперфузия в височно-теменной коре (17%); 4) гипоперфузия в лобной коре (17%).
При БПД перфузия в лобной, височной и теменной коре была достоверно ниже, чем при БП без деменции и МСА, но существенно не отличалась от церебральной перфузии ПНП или ДТЛ. При БПД прослеживалась выраженная тенденция к снижению уровня перфузии в затылочной коре по сравнению с БП без деменции, хотя она и не достигла порога статистической значимости (р=0,09).
У больных с ДТЛ чаще всего выявлялось 2 типа изменений: 1) двустороннее диффузное снижение перфузии (44%); 2) двустороннее снижение перфузии в височно-теменно-затылочных отделах (33%). У единичных больных отмечались также два других типа изменений: 1) снижение перфузии преимущественно в лобных отделах; 2) снижение перфузии в основном в височно-теменной области. Снижение перфузии в лобной, височной и теменной коре при ДТЛ было выше, чем при БП без деменции, однако существенно не отличалось от аналогичного показателя при БПД. Состояние перфузии в лобной и височной коре у больных ДТЛ коррелировало с общей оценкой когнитивных нарушений по ШДМ (r=0,4; р<0,05) и поведенческих нарушений (r=-0,3; р<0,05).
Установлена негативная корреляция между наличием психотических симптомов (зрительных галлюцинаций, параноидного бреда) у больных БПД и ДТЛ и перфузией правой (r= -0,4; р<0,05), но не левой височной коры. В то же время ДТЛ не отличалась от БП, МСА и ПНП по выраженности снижения перфузии стриатума и таламуса.
В последние годы за рубежом для диагностики паркинсонизма используются различные методы функциональной нейровизуализации, прежде всего позитронно-эмиссионная томография (ПЭТ) и ОФЭКТ, которые позволяют исследовать распределение тех или иных радиофармпрепаратов и тем самым оценивать сохранность пре- или постсинаптических структур в различных нейромедиаторных системах. Но их крайне высокая стоимость не позволяет применять их в клинической практике, к тому же их дифференциально-диагностическое возможности оказались весьма ограниченными [1, 13, 15,22,43, 47, 50]. Мы изучали более доступный для клинической практики метод исследования - ОФЭКТ с 99mТс-ГМАПО (церетек), позволяющий оценить степень региональной перфузии различных отделов коры большого мозга и подкорковых структур [27].
Результаты показывают, что отсутствие существенных изменений перфузии коры больших полушарий при ОФЭКТ с 99mТс-ГМПАО коррелирует с отсутствием деменции и свидетельствует в пользу БП или МСА. При сочетании паркинсонизма и деменции диспропорциональное снижение перфузии лобной коры является аргументом в пользу ПНП или (по данным литературы) лобно-височной деменции с паркинсонизмом, тогда как диффузное снижение перфузии коры больших полушарий или снижение перфузии в задних отделах коры больших полушарий более характерно для БПД, ДТЛ и БА с паркинсонизмом.
Важно подчеркнуть однотипность нейровизуализационных изменений при БПД и ДТЛ, что наряду с близостью профиля нейропсихологических нарушений [3] может быть дополнительным аргументом в пользу нозологической близости двух этих состояний. В то же время для БА с паркинсонизмом характерно заметно выраженное снижение перфузии в височных отделах на фоне более сохранной перфузии лобной и затылочной коры.
Ни при одном из заболеваний мы не выявили корреляции между наличием на МРТ сосудистых изменений и снижением перфузии в том или ином отделе мозга. В связи с этим можно полагать, что выявленное уменьшение перфузии корковых и подкорковых структур при нейродегенеративных заболеваниях, вызывающих паркинсонизм, отражают ослабление функциональной активности того или иного отдела мозга, которое, в свою очередь, может быть вызвано непосредственным вовлечением данной структуры в дегенеративный процесс либо ее деафферентацией [20, 27]. Важность второго механизма подчеркивается отсутствием статистически значимой корреляции между степенью снижения перфузии и выраженностью атрофических изменений, оцениваемых при МРТ с помощью визуальной рейтинговой шкалы [2, 14, 42]. В частности при ПНП значительное снижение перфузии лобных долей может отображать не только дегенеративные изменения в лобной коре, которые довольно умеренны, но также утрату афферентации от подкорковых и стволовых структур, а также зубчатого ядра мозжечка. Вместе с тем умеренное снижение перфузии в височной, теменной и затылочной коре может быть вызвано их разобщением с лобными долями [5, 12].
Снижение перфузии стриатума и таламуса при ПНП может свидетельствовать об утрате собственных нейронов, а также снижении афферентации от педункулопонтинного ядра и паллидоталамических путей. В связи с этим изменения региональной перфузии опережают по времени развитие структурных изменений, которые можно выявить на МРТ, и создают условия для более ранней нозологической диагностики паркинсонизма.
Мы установили, что ранним признаком МСА может быть снижение перфузии мозжечка, не наблюдавшееся ни при одном другом заболевании. В то же время у некоторых больных МСА с длительностью заболевания менее 2 лет выявлялась нормальная картина ОФЭКТ. Относительная сохранность церебральной перфузии различных отделов коры при МСА соответствует отсутствию грубого когнитивного дефекта [11, 52]. Важно отметить, что у части больных МСА с низкой перфузией мозжечка при МРТ не было выявлено выраженной атрофии мозжечковых структур. Таким образом, ОФЭКТ с 99mТс-ГМПАО является более чувствительным методом оценки состояния стволово-мозжечковых систем, чем МРТ.
У больных с ПНП отмечены обратная зависимость выраженности поведенческих нарушений от состояния перфузии лобной коры и прямая зависимость от состояния перфузии теменной коры. Подобная закономерность связана, возможно, с тем, что в патогенезе некоторых вариантов поведенческих нарушений, прежде всего полевого поведения и расторможенности, важную роль может играть вторичное растормаживание теменной коры вследствие дисфункции лобной коры [2, 10].
Полученные нами данные показывают, что гипоперфузия в лобных отделах на определенном этапе развития заболевания может быть важным дифференциально-диагностическим признаком, позволяющим различить ДТЛ и БА. При ДТЛ гипоперфузия лобной коры возникает на сравнительно ранней стадии заболевания, на фоне относительно мягкой деменции, а при БА развивается поздно и на фоне достаточно тяжелой деменции.
В ряде исследований отмечено, что гипоперфузия затылочной коры - один из характерных признаков БП и ДТЛ, позволяющих, в частности, дифференцировать их с БА. Мы отметили у больных БПД и ДТЛ лишь тенденцию к снижению уровня перфузии в затылочной коре по сравнению с БП без деменции и БА, которая, однако, не достигала порога статистической значимости. Гипоперфузия затылочной коры при БПД и ДТЛ может отражать ее дисфункцию, связанную с дофаминергической или холинергической денервацией. Тем не менее связать гипоперфузию затылочной коры с какими-либо специфическими когнитивными или поведенческими расстройствами нам не удалось. В то же время мы выявили корреляцию между наличием психотических симптомов и гиноперфузией правой, но не левой височной коры. Особая роль правого полушария в развитии психотической симптоматики отмечена и некоторыми другими авторами [41, 42].
Значительное сходство профиля перфузионных изменений при БПД и ДТЛ, наряду с близостью нейропсихологических изменений, может служить дополнительным аргументом в пользу нозологической близости двух заболеваний [3].
Проведенное нами исследование показало, что данные ОФЭКТ в комплексе с клиническими и нейропсихологическими данными могут иметь важное дифференциально-диагностическое значение при нозологической диагностике паркинсонизма, особенно на ранней стадии его развития.
Литература
1. Голубев В.Л., Левин Я.И., Вейн A.M. Болезнь Паркинсона и синдром паркинсонизма / М.: МЕДпресс, 1999.
2. Левин О.С. Клинико-нейропсихологические и нейровизуализационные аспекты дифференциальной диагностики паркинсонизма: Дисс. д-ра мед.наук. -М., 2003.
3. Левин О.С., Амосова Н.А., Наймушина Т.В., Смоленцева И.Г. Сравнительное клинико-нейропсихо-логическое исследование больных болезнью Паркинсона и деменцией с тельцами Леви.// Журн. неврол. и психиатр, им. Корсакова. - 2004 - №1 - С. 37-42.
4. Левин О.С., Федорова Н.В., Шток В.Н. Дифференциальная диагностика паркинсонизма. // Журн. неврол. и психиатр, им. Корсакова. - 2003. - №3. - С.54-60.
5. Лурия А.Р. Основы нейропсихология. - М., МГУ, 1973.
6. Шток В.Н., Левин О.С., Федорова Н.В. Экстрапирамидные расстройства. - М.: МИА, 2002.
7. Шток В.Н., Федорова Н.В. Лечение паркинсонизма. - М., 1997.
8. Яхно Н.Н. Актуальные вопросы нейрогериатрии / В кн.: Достижения в нейрогериатрии. - М., 1995. - С.9-27.
9. Яхно Н.Н., Дамулин И.В., Гончаров О.А. Сравнительная оценка различных форм паркинсонизма у больных пожилого и старческого возраста. // Журн. неврол. и психиатр, им. С.С.Корсакова. - 1992. - Т.92. - № 1. - С.67-72.
10. Agid Y., Javoy-Agid К, Ruberg M. et al. Progressive supranuclear palsy: anatomo-clinical and biochemical considerations. // Adv. Neurol. - 1986. -Vol. 45. -P. 191-206.
11. AlbaneseA., Colosimo C., Bentivoglio A.R. etal. Multiple system atrophy presenting as parkinsonism // J. Neurol. Neurosurg. Psychiatry. - 1995. - Vol. 59. - P.144-151.
12. Alexander G.A., DeLong M.R. Central mechanism of initiation and control of movement // In: A.K.Asbury, G.M.McKhann, W.I.McDonald (eds). Diseases of Nervous System. Clinical Neurobiology. 2-ed. Philadelphia, WB Saunders, 1992. - P.285-308.
13. Antonini A., Leenders K.L., Vontobel P. et al. Complementary PET studies of striatal neuronal function in the differential diagnosis between multiple atrophy and Parkinson's disease // Brain. - 1997. - Vol.120. - P.2187-2192.
14. Ballan G., Yekhlef R, Macia F. et al. Routine MRI in multiple system atrophy, progressive supranuclear palsy and corticobasal degeneration:differential diagnosis clues with Parkinson's disease// Mov.disord. - 2000. - Vol.15 (Suppl.3). - P. 205.
15. Brooks D.J. Functional imaging of movement disorders / In: C.D.Marsden, S.Fahn (eds). Movement disorders 3. Cambrridge, Butterworth Heinemann, 1994. - P.46-64.
16. Brooks D.J. The early diagnosis of Parkinson's disease// Ann. Neurol. 1998. - 44 (Suppl. 1):S10-S18.
17. Burn D.J., Sawle G. V., Brooks D.J. Differential diagnosis of Parkinson disease, multiple system atrophy, and Steele-Richardson-Olszewski syndrome: discriminant analysis of striatal 18F-dopa PET data. // J. Neurol. Neurosurg. Psychiatry. - 1994. - Vol. 57. - P.278-284.
18. Dagher A. Functional imaging in Parkinson's disease. // Semin. Neurol. - 2001. -Vol. 21.-P.23-32.
19. Davie C.A., Barker G.J., Machado C., Miller D.H., Lees A J. Proton magnetic resonance spectroscopy in Steele-Richardson-Olszewski syndrome. // Mov. Disord. - 1997. - Vol. 12. - P.767-771.
20. Defebvre L, Lecouffe P., Destee A. et al. Tomographic measurements of regional cerebral blood flow in progressive supranuclear palsy and Parkinson's disease. // Acta Neurol. Scand. - 1995. - Vol. 92. - P.235-241.
21. DeRijk M.C., Tzourio C., Breteler M.M. et al. Prevalence of parkinsonism and Parkinson's disease in Europe: the EUROPARKINSON Collaborative Study. European Community Concerted Action on the Epidemiology of Parkinson's Disease. // J. Neurol. Neurosurg. Psychiatry. - 1997. - Vol. 62. - P.10-15.
22. EidelbergD. Differential diagnosis of parkinsonism with [18F]-fluorodeoxyglucose (FDG) and PET. // Mov. Disord. - 1996.-Vol. 11.-P.349.
23. Fahn S., Elton R. Unified Parkinson's disease rating scale. Recent developments in Parkinson's disease. // Fahn S., Marsden C, Calne D. et al. (Eds). McMillan Healthcare Information. - 1987. - Vol. 5. - P.153-163.
24. Gibb W., Lees A. Relevance Lewy body pathogenesis of idiopathic Parkinson's disease// J. Neurol. Neurosurg. Psychiatry. - 1988. - Vol. 51. - P.745-752.
25. Gilinan S., Low P.A., Quinn N. Consensus statement on the diagnosis of multiple system atrophy. // J. Auton. Nerv. Syst. - 1998. - Vol. 74. - P.189-192.
26. Golbe L.I. Epidemiology of movement disorders. // In: J. Jankovic, E.Tolosa (eds). Parkinson's disease and movement disorders. 3-nd ed. - Baltimore. Williams&Wilkins, 1998. - P.119-132.
27. Hubert M.O., Smampinato U., Mas J.L. et al. A comparative technetium 99m hexamethylpropylene amine oxime SPET [sic] study in different types of dementia. // Eur. J. Nucl. Med.. - 1991. -Vol.18. - P.3-11.
28. Hoehn M., Jahr M.D. Parkinsonism: onset, progression and mortality // Neurology. - 1967. - Vol. 17. - P. 427-442.
29. Hughes A.J., Daniel S.E., Blankson S. et al. A clinicopathologic study of 100 cases of Parkinson's disease. // Arch. Neurol. - 1993. - Vol. 50. - P.140-148.
30. Jankovic J., Rajput A.H., McDermott M.P. et al. The evolution of diagnosis in early Parkinson's disease. Parkinson Study Group. // Arch. Neurol. - 2000.- Vol. 57. - P.369-372.
31. Jellinger K. The pathology of parkinsonism. // In: Movement disorders 2. Eds. C.D.Marsden, S.Fahn. Butterworth. - 1987. - P.124-165.
32. Konagaya M., Konagaya Y., lida M. Clinical and magnetic resonance imaging study of extrapyramidal symptoms in multiple system atrophy. // J. Neurol. Neurosurg. Psychiatry. - 1994.- Vol. 57.-P.1528-1531.
33. Litvan L, Agid Y., Calne D., et al. Clinical research criteria for the diagnosis of progressive supranuclear palsy (Steele-Richardson-Olszewski syndrome): report of the NINDS-SPSP international workshop. // Neurology. - 1996. - Vol. 47. - P.1-9.
34. Litvan 1. Parkinsonism-Dementia syndromes // In: J.Jankovic, E.Tolosa (eds). Parkinson's disease and movement disorders. 3-nd ed. - Baltimore. Williams&Wilkins, 1998. - P.245-262.
35. Litvan I., Bhatia K.P., Burn D.J. et al. Sic task force appraisal of clinical diagnostic criteria for parkinsonian disorders. // Mov. Disord. - 2003. - Vol. 18. - P. 467-486.
36. Marek K., Seibyl J., Shoulson I. et al. Dopamine transporter brain imaging to assess the effects of pramipexole versus levodopa on Parkinson disease progression. // J.A.M.A. - 2002. - Vol. 387. - P. 1653-1661.
37. Mattis S. Dementia Rating Scale: Professional manual. // Odessa, FL: Psychological assessment resources, 1988.
38. McKeith I.G., Galasko D., Kosaka K. et al. Consensus guidlines for the clinical and pathologic diagnosis of dementia with Lewy bodies. // Neurology. - 1996. - Vol. 47. - P. 113-1124.
39. McKhann G., Drachman D., Folstein M. et al. Clinical diagnosis of Alzheimer's disease: report of the NINCDS-ADRDA work group under the auspices of Department of health and human survices task force on Alzheimer's disease. // Neurology. - 1984. - Vol. 34. - P. 939-944.
40. Messa C., Volonte M.A., Fazio F. et al. Differential distribution of striatal [123I]beta-CIT in Parkinson's disease and progressive supranuclear palsy, evaluated with single-photon emission tomography. // Eur. J. Nucl. Med. - 1998. - Vol. 25. - P.1270-1276.
41. Okuda В., Tachibana H., Kawabata K. et al. Comparison of brain perfusion in corticobasal degeneration and Alzheimer's disease. // Dement. Geriatr. Cogn. Disord. - 2001. - Vol. 12. - P.226-231.
42. Pantelis C., Velakoulis D., McGorry P.O. et al. Neuroanatomical abnormalities before and after onset of psychosis: a cross-sectional and longitudinal MRI comparison. // Lancet. - 2003. - Vol. 361. - P.281-288.
43. Pirker W., Asenbaum S., Bencsits G. et al. [123I]beta-CIT SPECT in multiple system atrophy, progressive supranuclear palsy, and corticobasal degeneration. // Mov. Disord. - 2000. - Vol. 15.-P.1158-1167.
44. Quinn N. Multiple system atrophy: the nature of the beast // J. Neurol. Neurosurg. Psychiatry. - 1989. - Vol. 52 (special suppl.). - P.262-281.
45. Savoiardo M., Strada L., Girotti F. et al. Olivopontocerebellar atrophy: MR diagnosis and relationship to multiple system atrophy. // Radiology. - 1990. - Vol. 174. - P.693-696.
46. Schulz J.B., Klockgether Т., Petersen D. et al. Multiple system atrophy: natural history, MRI morphology, dopamine receptor imaging with 123IBZM-SPECT // J. Neurol. Neurosurg. Psychiatry. - 1995. - Vol. 59. - P.144-151.
47. Seppi K., Schocke M., Esterhammer R., et al. Diffusion-weighted imaging discriminates PSP from PD but not fron Parkinson variant of MSA. // Neurology, 2003. - Vol. 60. - P.589-598.
48. Stacy M., Jankovic J. Differential diagnosis of Parkinson's disease and parkinsonism-plus syndromes // Neurol.Clin. - 1992. - Vol. 10. - P.341-359.
49. Stern M.B., Braffman B.H., Skolnick B.E. et al. Magnetic resonance imaging in Parkinson's disease and parkinsonian syndromes. // Neurology. - 1989. - Vol. 39. - P.1524-1526.
50. Takatsu H., Nagashima K., Murase M. et al. Differentiating Parkinson's disease from multiple-system atrophy by measuring cardiac iodine-123 metaiodobenzylguanidine accumulation. // J.A.M.A. - 2000. - Vol. 284. - P.44-45.
57. Tedeschi G., Litvan L, Bonavita S. et al. Proton magnetic resonance spectroscopic imaging in progressive supranuclear palsy, Parkinson's disease and corticobasal degeneration. // Brain. - 1997. - Vol. 120. - P.1541-1552.
52. Wenning G.K., Tison F., Elliot L. et al. Olivopontocerebellar pathology in multiple system atrophy. // Mov.disord. - 1996. - Vol. 11. - P.157-162.
Левин О.С., Амосова И.А., Поцыбина В.В., Смоленцева И.Г., Олюнин Д.Ю. Роль однофотонной эмиссионной компьютерной томографии с 99mТс-ГМАПО в нозологической диагностике паркинсонизма // Неврологический вестник. - 2005. - Т. XXXVII, вып. 1-2. - С.5-12.